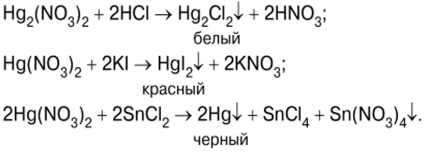
Phản ứng của các hợp chất thủy ngân
Thủy ngân kim loại và các hợp chất của nó rất độc đối với các sinh vật sống. Điều này đặc biệt đúng đối với các hợp chất hòa tan nhiều trong nước. Cần hết sức thận trọng khi thử nghiệm với sự kết hợp của nguyên tố độc nhất này (thủy ngân là kim loại duy nhất ở thể lỏng ở nhiệt độ phòng). Tuân thủ các giới luật cơ bản của một nhà hóa học? sẽ cho phép bạn tiến hành một số thí nghiệm với các hợp chất thủy ngân một cách an toàn.
Trong thí nghiệm thứ nhất, ta thu được hỗn hống nhôm (dung dịch của kim loại này trong thủy ngân lỏng). Dung dịch thủy ngân (II) Hg nitrat (V) Hg (NO3)2 và một đoạn dây nhôm (ảnh 1). Một thanh nhôm (đã được rửa sạch cặn bẩn cẩn thận) cho vào ống nghiệm đựng dung dịch một muối thuỷ ngân hoà tan (ảnh 2). Sau một thời gian, ta có thể quan sát thấy bọt khí thoát ra trên bề mặt dây dẫn (ảnh 3 và 4). Sau khi lấy que ra khỏi dung dịch, thấy đất sét được phủ một lớp lông mịn, ngoài ra chúng ta còn thấy những quả bóng bằng kim loại thủy ngân (ảnh 5 và 6).
Hóa học - kinh nghiệm kết hợp thủy ngân
Trong điều kiện bình thường, bề mặt của nhôm được phủ một lớp nhôm oxit rất khít.2O3cách ly hiệu quả kim loại khỏi các ảnh hưởng tích cực từ môi trường. Sau khi làm sạch và nhúng thanh vào dung dịch muối thủy ngân, các ion Hg bị dịch chuyển2+ nhôm hoạt động hơn
Thủy ngân lắng đọng trên bề mặt thanh tạo thành hỗn hống với nhôm, làm cho oxit khó bám vào nó. Nhôm là một kim loại rất hoạt động (nó phản ứng với nước để giải phóng hydro - bọt khí được quan sát thấy), và việc sử dụng nó như một vật liệu cấu trúc là có thể do lớp phủ oxit dày đặc.
Trong thí nghiệm thứ hai, chúng ta sẽ phát hiện ra các ion amoni NH.4+ sử dụng thuốc thử của Nessler (nhà hóa học người Đức Julius Nessler là người đầu tiên sử dụng nó trong phân tích vào năm 1856).
Thí nghiệm về phản ứng của hoa bia và hợp chất của thủy ngân
Thử nghiệm bắt đầu bằng sự kết tủa của thủy ngân (II) iodua HgI.2, sau khi trộn các dung dịch kali iođua KI và thủy ngân (II) nitrat (V) Hg (NO3)2 (ảnh 7):
Kết tủa màu đỏ da cam của HgI2 (ảnh 8) sau đó được xử lý bằng lượng dư dung dịch kali iođua để thu được một hợp chất phức dễ tan có công thức K2HgI4 ? Kali tetraiodercurate (II) (Ảnh 9), là thuốc thử của Nessler:
Với hợp chất tạo thành, chúng ta có thể phát hiện ra các ion amoni. Vẫn cần dung dịch natri hydroxit NaOH và amoni clorua NH.4Cl (ảnh 10). Sau khi thêm một ít dung dịch muối amoni vào thuốc thử Nessler và kiềm hóa môi trường bằng bazơ mạnh, ta quan sát thấy chất trong ống nghiệm có màu vàng cam. Phản ứng hiện tại có thể được viết là:
Hợp chất thủy ngân thu được có cấu trúc phức tạp:
Thử nghiệm Nessler có độ nhạy cao được sử dụng để phát hiện ngay cả dấu vết của muối amoni hoặc amoniac trong nước (ví dụ: nước máy).

